পর্যায়বৃত্ত ধর্ম: তড়িৎ ঋণাত্নকতা আমাদের আজকের আলোচনার বিষয়। এই পাঠটি “এইচএসসি রসায়ন ১ম পত্র” এর “পর্যায় সারণি ও মৌলের পর্যাবৃত্ত ধর্ম” ইউনিট ২ এর অন্তর্ভুক্ত
পর্যায়বৃত্ত ধর্ম: তড়িৎ ঋণাত্নকতা
তড়িৎ ঋণাত্মকতা বা ইলেকট্রোনেগেটিভিটি
(Electronegativity)
সমযোজী বন্ধন গঠিত হয় বন্ধনে অংশগ্রহণকারী দুটি পরমাণুর একটি করে ইলেকট্রন শেয়ারের মাধ্যমে। যদি বন্ধনে অংশগ্রহণকারী পরমাণু দুটির ইলেকট্রনের প্রতি আসক্তি একই হয় তবে শেয়ারকৃত ইলেকট্রন যুগল উভয় পরমাণুর মাঝখানে থাকবে কিন্তু পরমাণু দুটির ইলেকট্রন আসক্তির মান যদি একই না হয় তবে যেটির ইলেকট্রন আসক্তির মান বেশি হবে শেয়ারকৃত ইলেকট্রন যুগল তার দিকে বেশি আকৃষ্ট হবে। অর্থাৎ সমযোজী বন্ধনে শেয়ারকৃত ইলেকট্রন জোড়কে কোনো পরমাণুর নিজের দিকে টেনে নেওয়ার প্রবণতাকে ঐ পরমাণুর তড়িৎ ঋণাত্মকতা বা ইলেকট্রোনেগেটিভিটি বলা হয় ।
সংজ্ঞা : কোনো একটি সমযোজী যৌগের অণুতে উপস্থিত দুটি ভিন্ন মৌলের পরমাণুর মধ্যে শেয়ারকৃত ইলেকট্রন জোড়কে একটি পরমাণু কর্তৃক নিজের দিকে অধিক আকর্ষণ করার তুলনামূলক ক্ষমতাকে সেই মৌলের তড়িৎ ঋণাত্মকতা বলা হয় ।
হাইড্রোজেন এবং ফ্লোরিন ইলেকট্রন শেয়ারের মাধ্যমে হাইড্রোজেন ফ্লোরাইড (HF) অণু গঠন করে। ফ্লোরিনের ইলেকট্রনের প্রতি আসক্তি হাইড্রোজেন অপেক্ষা বেশি হওয়ায় শেয়ারকৃত ইলেকট্রন জোড় ফ্লোরিনের দিকে বেশি পরিমাণে আকৃষ্ট হয়।
![]()
HF যৌগে H এবং F পরমাণুর অসম ইলেকট্রোনেগেটিভিটির কারণে HF অণুতে হাইড্রোজেন পরমাণুতে আংশিক ধনাত্মক চার্জ +8 -8
( H) এবং ফ্লোরিন পরমাণুতে আংশিক ঋণাত্মক চার্জের ( F) সৃষ্টি হয়। অণুতে এরুপ চার্জের সৃষ্টি হলে এ ধরনের অণুকে পোলার অণু বলে ।
মৌলের পরমাণুর আকার হ্রাস এবং নিউক্লিয়াসে চার্জ বৃদ্ধিতে তড়িৎ ঋণাত্মকতা বৃদ্ধি পায় ।
মৌলের তড়িৎ ঋণাত্মকতা একটি পর্যায়বৃত্ত ধর্ম। একই গ্রুপে পারমাণবিক সংখ্যা বৃদ্ধিতে মৌলের তড়িৎ ঋণাত্মকতার মান হ্রাস পায়। একই শ্রেণিতে পারমাণবিক সংখ্যা বৃদ্ধির সাথে সাথে প্রত্যেকটি পরমাণুতে একটি করে নতুন শক্তিস্তর যুক্ত হয় ফলে পরমাণুর আকার বৃদ্ধি পায় । পরমাণুর আকার বৃদ্ধির সাথে সাথে বন্ধনে শেয়ারকৃত ইলেকট্রন জোড় নিউক্লিয়াস হতে ক্রমশ দূরে অবস্থান করে। ফলে ইলেকট্রন জোড়ের উপর নিউক্লিয়াসের আকর্ষণ হ্রাস পায়। পর্যায় সারণির গ্রুপ-17 মৌলের তড়িৎ ঋণাত্মকতার মান নিরূপ :
F = 4.0 ; Cl = 3.0; Br = 2.8; I = 2.5; At = 2.0
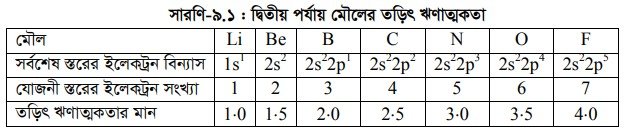
আবার, পর্যায় সারণির কোনো একটি নির্দিষ্ট পর্যায়ে বাম দিক থেকে যতই ডানদিকে যাওয়া যায় পারমাণবিক সংখ্যা বৃদ্ধির সাথে সাথে মৌলের তড়িৎ ঋণাত্মকতা ততই বৃদ্ধি পায়। একই পর্যায়ে মৌলসমূহের পারমাণবিক সংখ্যা বৃদ্ধির সাথে কোনো নতুন শক্তিস্তর বৃদ্ধি পায় না অথচ একই শক্তিস্তরে পর্যায়ক্রমে প্রত্যেকটি মৌলের পরমাণুর নিউক্লিয়াসে একটি করে প্রোটন এবং বহিস্থ শক্তিস্তরে একটি করে ইলেকট্রন যুক্ত হয়। পরমাণুর নিউক্লিয়াসের চার্জ বৃদ্ধি হওয়ায় সর্বশেষ শক্তিস্তরের উপর নিউক্লিয়াসের আকর্ষণ বৃদ্ধি পায়। ফলে পরমাণুর আকার ক্রমশ হ্রাস পায়। পরমাণুর আকার ক্রমশ হ্রাস পাওয়ায় সমযোজী বন্ধনে শেয়ারকৃত ইলেকট্রনের উপর নিউক্লিয়াসের আকর্ষণ বৃদ্ধি পায়। এ কারণে মৌলের তড়িৎ ঋণাত্মকতা বৃদ্ধি পায়। পর্যায় সারণির ২য় পর্যায়ের মৌলসমূহের তড়িৎ ঋণাত্মকতার মান নিম্নরূপ :
Li = 1-0 ; Be = 1.5; B = 2.0, C = 2-5; N = 3-0; O = 3.5; F = 4.0
পর্যায় সারণিতে মৌলের তড়িৎ ঋণাত্মকতার মান দেখানো হলো :
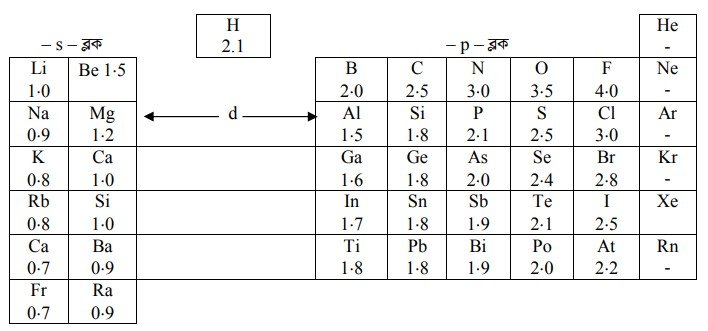
তড়িৎ ঋণাত্মকতার উপর বিভিন্ন নিয়ামকের প্রভাব
Effect of Different Factors on EN
সমযোজী বন্ধনে অংশগ্রহণকারী পরমাণুদ্বয়ের শেয়ারকৃত ইলেকট্রন একটি পরমাণু কর্তৃক নিজের দিকে টেনে নেওয়ার তুলনামূলক ক্ষমতাকে ঐ পরমাণুর তড়িৎ ঋণাত্মকতা বলে । মৌলের তড়িৎ ঋণাত্মকতা যেসব নিয়ামক দ্বারা প্রভাবিত হয় তা হলো-
(i) পরমাণুর আকার
(ii) উপস্তর এবং
(iii) ইলেকট্রন বিন্যাস।
নিম্নে নিয়ামকসমূহের প্রভাব বর্ণনা করা হলো :
(i) পরমাণুর আকার (Size of Atom) :
পরমাণুর আকার বৃদ্ধিতে পরমাণুর নিউক্লিয়াস হতে সর্বশেষ শক্তিস্তর দূরে সরে যায় তাই বন্ধনে অংশগ্রহণকারী শেয়ারকৃত ইলেকট্রন জোড়ের উপর নিউক্লিয়াসের আকর্ষণ হ্রাস পায় এবং পরমাণুর তড়িৎ ঋণাত্মকতা হ্রাস পায়। গ্রুপ-17 এর মৌলসমূহের তড়িৎ ঋণাত্মকতার মান নিম্নে দেওয়া হলো :
F = 4-0; Cl = 3-0; Br = 2-8; I = 2.5; At = 2.2
(১) নিউক্লিয়ার চার্জ (Nuclear Charge) : পরমাণুর নিউক্লিয়ার চার্জ বৃদ্ধির সাথে মৌলের ইলেকট্রোনেগেটিভিটি সম্পর্কিত। নিউক্লিয়ার চার্জ যত বেশি হবে ঐ নিউক্লিয়ার কর্তৃক সর্বশেষ স্তরের ইলেকট্রনের প্রতি আকর্ষণ তত বেশি প্রবল হয়। দ্বিতীয় পর্যায়ের মৌলসমূহের Li(3) হতে F(7) পর্যন্ত ক্রমান্বয়ে নিউক্লিয়াসে একটি করে প্রোটন যুক্ত হয় এবং শেষ শক্তিস্তরে একটি করে ইলেকট্রন যুক্ত হয় অর্থাৎ ক্রমান্বয়ে পারমাণবিক সংখ্যা বৃদ্ধিতে নিউক্লিয়ার চার্জ বৃদ্ধি পায় এবং মৌলের তড়িৎ ঋণাত্মকতার মানও বৃদ্ধি পেতে থাকে ।